■ここ数年で大きなコストダウンに成功
●電動車のもっとも重要な部品のひとつ
電動車にとって、車載2次電池はもっとも重要な部品のひとつです。電気エネルギーを供給する放電や、逆に得られたエネルギーを電気として充電する役目を担っています。
標準車の鉛蓄電池と、電動車で使われているニッケル水素電池、イオンリチウム電池の違いについて、解説していきます。
●2次電池の基本
自動車用の電池は、正極と負極で別々に起こる酸化・還元反応を利用した化学電池で、充電による蓄電ができる2次電池です。充電することによって電気エネルギーを化学エネルギーの形で蓄え、放電時には化学エネルギーを再度電気エネルギーに変換して、充放電を繰り返すことができます。
電池の能力を示す指標には、次のようなものがあります。
・バッテリ容量 (Ah)
蓄電可能なエネルギーで、一定の電流値で何時間放電できるかの指標です。例えば、容量10Ahとは、10Aの放電を1時間持続できる電気エネルギーを示しています。
・充電率 (%)
満充電100%に対する充電量の割合を、充電率(SOC:State of Charge)として表します。
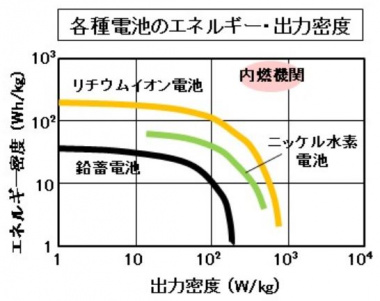
・エネルギー密度 (Wh/kg)
電池重量あたりの蓄電可能なエネルギーです。EVでは、満充電時の航続距離に関係します。
・出力密度 (W/kg)
電池重量あたりの瞬時に入出力できる電力です。瞬発力、加速性能を示すので、HEVで重視されます。
●鉛蓄電池とは
鉛蓄電池は、安価で信頼性に優れ、エンジン車では標準的に使用されています。一方、繰り返し充電することによって、負極に硫酸鉛の結晶が発生しやすく、性能が低下しやすい欠点があります。したがって、充放電量には制約があり、過放電にならないように制御する必要があります。
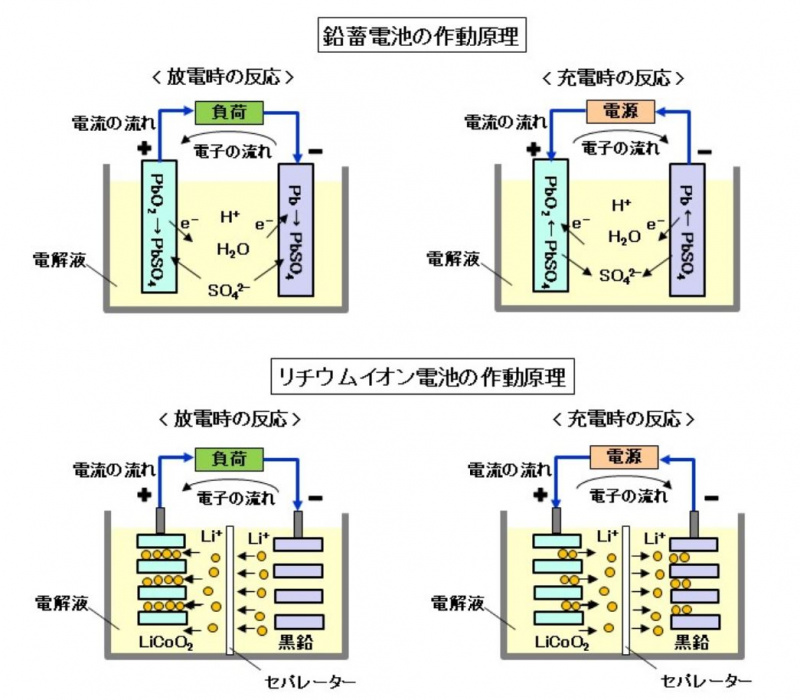
正極は二酸化鉛PbSO2、負極は金属鉛Pb、電解質は希硫酸H2SO4で構成され、充放電では以下の化学反応が起こります。
放電) Pb + PbO2 → 2PbSO4 + 2H2
充電) Pb + PbO2 ← 2PbSO4 + 2H20
ここで、放電時は負極で電子を与える酸化反応、正極で電子を受け取る還元反応が起こり、電子が負極から正極に移動し、電流が流れます。充電時はこれと逆の反応となり、逆方向に電子が流れ、電流が流れます。
●ニッケル水素電池とは
トヨタのプリウスHEVで使用しているニッケル水素電池は、エネルギー密度は後述のリチウムイオン電池に劣りますが、安全性が高いのが特徴です。
正極に水酸化ニッケル、負極に水素吸蔵合金、電解質として水酸化カリウムを用います。
放電) MH + NiOOH → M + Ni(OH)2 充電) MH + NiOOH ← M + Ni(OH)2
放電時には水素イオンが負極から正極へ、充電時には正極から負極へ移動し、充放電を繰り返します。
●リチウムイオン電池とは
リチウムイオン電池は、軽量で高性能(エネルギー密度がニッケル水素電池の約2倍)の電池で、EVのほとんどが採用しています。ただし、過充電と過放電に弱いため、高精度の制御や保護回路が必要です。特に過充電では、短絡によって発火や破裂の危険があります。
正極にリチウム系材料、負極にカーボン系材料、電解質としてリチウムイオンを含む電解質を用います。正極にコバルト酸リチウム、負極に炭素、電解質に有機電解液を使用した場合を例に示します。
放電) 6C + LiCoO2 → LinC6 + Li(1-X)CoO2 充電) 6C + LiCoO2 ← LinC6 + Li(1-X)CoO2
放電時にはイオン化したリチウムイオンが負極から正極へ、充電時にはリチウムイオンが正極から負極へ移動して、充放電を繰り返します。
●全固体電池
最近、正極と負極間に電解液を使わず、一種のセパレータだけがある全固体電池が注目されています。エネルギー密度の大幅な向上や安全性の向上、急速充電の実現などのメリットがあり、EVの普及を大きく加速することが期待されています。
EVの課題のひとつは、電池のコストですが、電池パックコストは2010年の11万円/kWh程度から、2016年には約3万円/kWhに、この6年間で1/4まで低下しました。
NEDO(新エネルギー・産業技術総合開発機構)の2025年の目標は1.5万円/kWhですから、EV普及のためには、さらなる低減が必要です。
(Mr.ソラン)
あわせて読みたい
from clicccar.com(クリッカー) http://bit.ly/2vrlAn4
via IFTTT http://bit.ly/2vrlAn4
コメント
コメントを投稿